![]()
Evaluación de los Niños Tratados en Nuestro Medio con Infusión Subcutánea Continua de Insulina
Objetivos: Analizar diversos aspectos epidemiológicos de la población infanto-juvenil con diabetes mellitus tipo 1 (DM1) en la que se inicia tratamiento con ISCI en las Unidades de Endocrinología Pediátrica de Cáceres y Badajoz, así como valorar la eficacia y características de esta terapia.
Pacientes y Métodos: Estudio analítico, observacional y retrospectivo de pacientes en los que se ha iniciado tratamiento con ISCI entre marzo de 2009 y diciembre de 2012. Analizamos indicaciones de esta terapia, HbA1c, dosis de insulina diaria, evolución del índice de masa corporal, número de controles glucémicos capilares diarios y complicaciones derivadas del tratamiento con bomba.
Resultados: De 283 pacientes con DM1 en seguimiento durante el tiempo de estudio, se instauró tratamiento con ISCI en 44 (27 niñas y 17 niños), con una edad media de 5,4 años (1,08-16,1 años) y un tiempo medio de evolución de la enfermedad de 3,83 años. Las indicaciones que motivaron el inicio de ISCI fueron hipoglucemias frecuentes en 36 pacientes (81,8%), inestabilidad glucémica en 25 (56,8%), bajas necesidades de insulina en 7 (15,9%), necesidad de flexibilizar horarios en 6 (13,6%), mal control metabólico en 5 (11,4%) y fenómeno del alba en 3 (6,8%). La HbA1c media previa fue de 7,08 %, 7,03% al año de ISCI, 6,98% a los 2 años y 6,96% a los 3 años, sin encontrarse diferencias significativas, aunque sí mejoró la HbA1c en 3 de los 5 pacientes en los que la indicación fue el mal control metabólico. La dosis de insulina diaria requerida fue menor durante el tratamiento con ISCI en comparación con múltiples dosis de insulina (MDI), aunque sin alcanzar la significación estadística. En todos los casos, salvo uno, se mantuvo la terapia con bomba, expresando las familias mejoría en la calidad de vida. Registramos dos episodios de cetosis, sin acidosis, secundarios a obstrucción del equipo de infusión, que precisaron asistencia en Urgencias.
Conclusiones: El tratamiento con ISCI resulta en nuestro estudio ser igual de efectivo que el tratamiento con MDI en términos de HbA1c. El tratamiento mediante ISCI puede considerarse como una adecuada alternativa al tratamiento con MDI del que se pueden beneficiarse un número importante de niños con DM1 independientemente de su edad o tiempo de evolución de su enfermedad si previamente son bien seleccionados para dicho tratamiento.
Objective: In this study, we aimed to analyse the demographic and clinical characteristics of a population of children with type 1 diabetes mellitus (DM1) treated with continuous subcutaneous insulin infusion (CSII). The efficiency and other characteristics of the therapy were also evaluated.
Methods: Retrospective observational study of patients attending the Paediatric Endocrinology Unit of Caceres and Badajoz, Spain, who started treatment with CSII between 2009 and 2012. The following variables were assessed: indication for treatment, HbA1c, daily insulin requirement, change in body mass index, daily frequency of capillary blood glucose measurements and complications of the pump system.
Results: From a total of 283 children with DM1 under follow-up during the study period, 44 started treatment with ISCI (27 females, 17 males). Mean age at treatment initiation was 5.4 years (1.08 – 16.1 years) and mean disease duration was 3.83 years. Indications for treatment were as follows: frequent hypoglycaemia in 36 cases (81.8%), glycaemic instability in 25 (56.8%), low insulin requirements in 7 (15.9%), inadequate metabolic control in 5 (11.4%), need for more flexible schedule in 6 (13.6%), and dawn phenomenon in 3 (6.8%). Mean HbA1c levels were 7.08% before treatment, 7.03% after one year of treatment, 6.98% after two years and 6.96% after three years. No significant differences were observed in terms of HbA1c levels before and after CSII; however, HbA1c levels improved in 3 out of 5 patients with an inadequate metabolic control pre-treatment. Daily insulin requirements decreased during CSII therapy as compared to multiple daily injections (MDI), although this change was not statistically significant. All patients except one continued on CSII therapy during the study period, with their relatives reporting an improvement in the quality of life. Two ketosis episodes, without acidosis, secondary to obstruction in infusion system, were observed in two patients who required assistance in Emergency Service.
Conclusions: Our study suggests that CSII may be as effective as MDI in terms of glycaemic control as measured by HbA1c levels. CSII may be considered as an adequate treatment alternative to MDI in previously selected patients with independence of age or illness evolution time.

17
Volumen XX Nº 2 Octubre 2013
E
VALUACIÓN
DE
LOS
N
IÑOS
T
RATADOS
EN
N
UESTRO
M
EDIO
CON
I
NFUSIÓN
S
UBCUTÁNEA
C
ONTINUA
DE
I
NSULINA
Key words: adolescents, children, continuous subcutaneous
insulin infusion, type 1diabetes mellitus.
Introducción
Los resultados del Diabetes Control and Complica-
tion Trial (DCCT)
(1,2)
y posteriormente, los del Epide-
miology of Diabetes Interventions and Complications
(EDIC) study
(3)
demostraron claramente la importancia
de mantener cifras de glucemia cercanos a la normali-
dad para evitar las complicaciones microvasculares que
aparecen en las personas con diabetes mellitus tipo 1
(DM1). El estudio DCCT evidenció que el grupo de ado-
lescentes también podía beneficiarse del buen control
metabólico y que esos beneficios se mantenían incluso
muchos años después de terminar el estudio a pesar de
que su control metabólico después del ensayo empeo-
rase
(4)
. En consecuencia, los objetivos del tratamiento
en niños y adolescentes con DM1 desde ese momento
fueron conseguir unos niveles de glucemia y hemoglo-
bina glicosilada (HbA1c) lo más cercanos a la normali-
dad desde el inicio de la enfermedad.
Sin embargo, en la fase inicial del DCCT se comunicó
un evento de hipoglucemia grave por paciente y año en
el grupo de adolescentes; un 39% de ellas con convul-
siones o coma
(3)
. Las frecuentes hipoglucemias asocia-
das a un control metabólico estricto suponían un factor
limitante para conseguir los objetivos marcados. El ob-
jetivo del tratamiento de la diabetes debe ser, por tanto,
conseguir y mantener un adecuado control metabólico,
minimizando el riesgo de hipoglucemia, para impedir o
retrasar la aparición de las complicaciones crónicas,
procurando la mejor calidad de vida posible.
Para conseguir el óptimo control metabólico de los
pacientes con DM1 se requiere una terapia de sus-
titución insulínica que se parezca lo más posible a los
perfiles que de esta hormona tienen los individuos sin
diabetes consistente en una secreción continua de in-
sulina entre comidas (secreción basal) y una secreción
aguda en respuesta a los alimentos (secreción prandial).
Esta forma de tratamiento insulínico, también llamada
terapia basal-bolo, puede llevarse cabo mediante múlti-
ples inyecciones diarias de insulina (MDI) o bien medi-
ante el empleo de infusión subcutánea continua de in-
sulina (ISCI).
Los primeros estudios con ISCI en pacientes con
DM1 a finales de los 70, si bien realizados en un número
reducido de pacientes y durante períodos de tiempo
muy limitados, pusieron de manifiesto la viabilidad de
esta terapia
(5, 6, 7)
. En los años 80, la experiencia en adul-
tos y adolescentes demostró que era bien tolerada y
permitía disminuir los valores de HbA1c, el número de
hipoglucemias y mejorar la calidad de vida del paciente.
Las limitaciones técnicas de los primeros modelos de
bomba y la falta de implicación de los clínicos fueron
los principales obstáculos para generalizar su uso en ni-
ños y adolescentes. El uso de la terapia con bomba de
insulina continuó siendo muy minoritario hasta que las
mejorías técnicas introducidas a partir de los años 90
consiguieron hacer de ellas un tratamiento más fácil y
seguro. Estas mejoras, junto con los resultados obteni-
dos en el DCCT, propiciaron que el empleo de la ISCI se
extendiera a adolescentes y, posteriormente, a niños de
menor edad. De hecho, los pacientes pediátricos con-
stituyen hoy en día el segmento poblacional con DM1
que experimenta mayor incremento en la instauración
del tratamiento con ISCI
(8)
.
En la actualidad hay un incremento ostensible en la
demanda de este tipo de terapia pero con una extraor-
dinaria y sorprendente diferencia entre la proporción
de pacientes con DM1 tratados con ISCI en España
en comparación con otros países de nuestro entorno.
Mientras que en nuestro país apenas llega al 3-4%, el
porcentaje de pacientes tratados con ISCI en Italia es
del 12% y en Holanda, Francia y Alemania se sitúa alre-
dedor del 20%. Solamente superamos las cifras de Por-
tugal y Rusia y estamos por debajo del porcentaje medio
de uso en la Unión Europea
(9, 10)
.
El objetivo de nuestro estudio es analizar diversos as-
pectos epidemiológicos de la población infanto-juvenil
con diabetes mellitus tipo 1 (DM1) en la que se inicia
tratamiento con ISCI en la Unidades de Endocrinología
Pediátrica de Cáceres y Badajoz, así como valorar la efi-
cacia y características de esta terapia.
Pacientes y Métodos
Realizamos un estudio observacional, analítico, longi-
tudinal y retrospectivo en las Unidades de Diabetes In-
fanto-Juvenil de los hospitales de Cáceres y Badajoz.
Fueron seleccionados aquellos pacientes con DM1 que
durante el período de tiempo comprendido entre marzo
de 2009 y diciembre de 2012 iniciaron tratamiento con
ISCI. De un total de 283 pacientes que a lo largo de di-
cho período fueron seguidos en las consultas de am-
bos hospitales, se instauró terapia con bomba infusora
de insulina en 44. Exceptuando dos pacientes en los
que el tratamiento con ISCI se inició ya durante la hos-
pitalización en el momento del debut, todos los pacien-
tes incluídos en el estudio habían realizado previamente
tratamiento intensivo con múltiples dosis de insulina,
incluyendo análogos de acción prolongada (glargina o
detemir) y de acción rápida (aspart, lispro o glulisina),
siendo este último el empleado en la bomba. Las mi-
croinfusoras empleadas fueron los modelos Paradigm®
(Medtronic) y Accu-Check ® (Roche). Fueron excluidos
del estudio aquellos pacientes que iniciaron el trata-
miento con ISCI antes y después del periodo citado de
reclutamiento.
La recogida de datos se efectuó mediante la revisión
de las historias clínicas de consulta de Endocrinología
Pediátrica y de hospitalización. Las variables evaluadas
fueron: edad al debut y al instaurar ISCI, indicaciones,
HbA1c antes y durante el tratamiento con ISCI, número
de controles glucémicos capilares al día, requerimientos
diarios de insulina, evolución del índice de masa corporal
y presentación de complicaciones graves.
Los motivos de instauración de ISCI recogidos en el
formulario de solicitud consensuado en la Comunidad
Autónoma de Extremadura incluyen:

18
S
OCIEDAD
DE
P
EDIATRÍA
DE
A
NDALUCÍA
O
CCIDENTAL
Y
E
XTREMADURA
Volumen XX Nº 2 Octubre 2013
– Mal control metabólico (HbA1c elevada), a pesar
del tratamiento intensivo optimizado con MDI (in-
cluidos análogos de acción rápida y retardada) y
colaboración apropiada por el paciente.
– Inestabilidad glucémica y/o perfil de glucemia caó-
tico (con HbA1c aceptable o buena) a pesar del
tratamiento intensivo optimizado con MDI (inclui-
dos análogos de acción rápida y retardada) y cola-
boración apropiada por el paciente.
– Hipoglucemias frecuentes, inadvertidas y/o limitan-
tes.
– Fenómeno del alba imposible de controlar con
cuatro dosis de insulina.
– Necesidad de flexibilizar horarios de inyecciones/
comidas por motivos laborales, etc (salvo si existe
buen control glucémico/metabólico sin hipogluce-
mias).
– Pacientes que hayan utilizado ininterrumpidamente
una bomba de insulina para el tratamiento de su
diabetes durante el menos los 12 meses previos.
– Planificación de gestación, sin lograr buen control
en tratamiento intensivo con MDI.
El protocolo de solicitud de tratamiento también re-
coge la posibilidad de especificar otras indicaciones
según criterio del facultativo.
Se consideraron criterios para no ofrecer el trata-
miento con ISCI:
– Falta de motivación y colaboración del paciente
y/o su familiar con mala adherencia al tratamiento.
– Inestabilidad psicológica y/o falta de expectativas
realistas.
– Problemas familiares o sociales que influyan en la
actitud hacia la diabetes.
Las determinaciones de HbA1c se realizaron en san-
gre capilar mediante los dispositivos Kit A1CNow+®
(Bayer) o DCA 2000+® (Bayer) de acuerdo con la es-
tandarización establecida por el DCCT. En la recogida
de datos se incluyeron los valores previos al inicio de
ISCI y, posteriormente, al año, a los 2 años y a los 3
años. Puesto que la determinación de HbA1c se re-
aliza en consulta con periodicidad trimestral, cada uno
de los valores recogidos (pre-ISCI, 1, 2 y 3 años post-
inicio ISCI) se obtuvo mediante la media aritmética de
tres cifras: la HbA1c correspondiente al momento anal-
izado, la previa (3 meses antes) y la posterior (3 meses
después) con objeto de que la cifra considerada fuese
más representativa del momento evaluado.
El índice de masa corporal (IMC), calculado como
el peso en kilogramos dividido entre el cuadrado de
la talla en metros, se expresó en desviaciones están-
dar (DE) respecto a la media según tablas de referencia
para la población española
(11)
.
Se consideraron complicaciones importantes la hi-
poglucemia grave (definida como aquella que cursa
con disminución del nivel de conciencia) y la cetoaci-
dosis diabética (glucemia > 200 mg/dl; pH < 7.30 y bi-
carbonato < 15 mEq/L y cuerpos cetónicos positivos
en sangre y/o orina).
Análisis Estadístico
El análisis estadístico se realizó mediante SPSS sta-
tistical package versión 19.0 para Windows (SPSS,
Inc., Chicago, IL, USA). Los datos referentes a vari-
ables cuantitativas se expresan como media ± DE y
los referentes a cualitativas en porcentajes. Se empleó
la prueba t de Student para muestras independientes
para comparar la cifra de HbA1c, requerimientos de in-
sulina, IMC y número de controles glucémicos capila-
res diarios, antes y después del inicio de tratamiento
con ISCI. Se consideró como significativa una p < 0,05.
Resultados
Durante el período de tiempo abarcado en el estu-
dio (marzo de 2009 a diciembre de 2012) 283 niños
y adolescentes con DM1 fueron seguidos en nuestros
servicios. De ellos, en 44 (15,5%), 27 niñas y 17 niños,
se instauró tratamiento con bomba infusora de insulina.
La edad media al inicio de la terapia fue de 5,4 años
(rango: 1,08-16,1 años). El tiempo medio de evolución
de la enfermedad al inicio de ISCI fue de 3,83 años
(rango: 0-9,9 años). Dos pacientes, ambos lactantes,
iniciaron tratamiento con bomba ya en el momento del
debut.
De la muestra de 44 pacientes, 27 habían comple-
tado al menos 1 año de tratamiento con ISCI al finalizar
el período de estudio evaluado, 17 al menos dos años,
y 10 completaron 3 años. Los dos pacientes que co-
menzaron tratamiento con bomba al debut fueron ex-
cluidos de la comparación de variables pre/post-inicio
de ISCI.
Las hipoglucemias frecuentes, inadvertidas y/o limi-
tantes fueron la principal razón para instaurar trata-
miento con ISCI (81,8% de los pacientes). La inesta-
bilidad glucémica supuso el segundo motivo más fre-
cuente (56,8%). Las restantes indicaciones fueron: ba-
jos requerimientos de insulina (15,9%), necesidad de
flexibilizar horarios (13,6%), mal control metabólico
(11,4%) y fenómeno del alba de difícil control (6,8%).
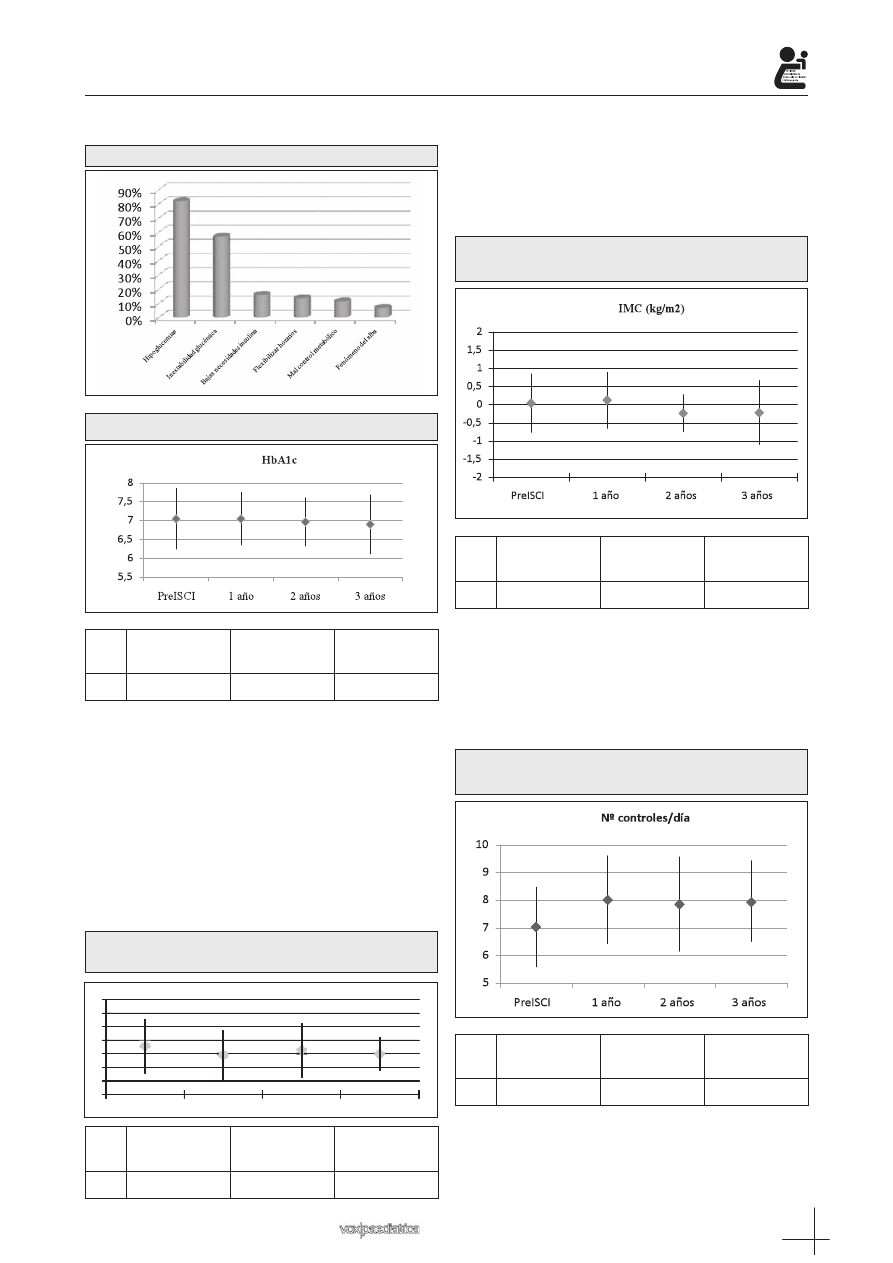
Los datos quedan reflejados en la figura 1.
La mayoría de los pacientes cumplían más de uno de
los criterios para ser incluídos en el tratamiento con ISCI.
La HbA1c media previa al inicio de ISCI fue de 7,08%
± 0,75. Un año después, la HbA1c media fue de 7,03%
± 0,76. A los 2 años, fue de 6,98% ± 0,72. Tras 3 años
de tratamiento con ISCI, la HbA1c media fue de 6,96%
± 0,70. Si bien existe una tendencia descendente en
las cifras de HbA1c antes y después de la instaura-
ción de ISCI, la diferencia no alcanza la significación
estadística (figura 2). No obstante, se constató mejoría
de la HbA1c en 3 de los 5 pacientes en los que el mal
control metabólico había sido criterio de indicación.
19
Volumen XX Nº 2 Octubre 2013
E
VALUACIÓN
DE
LOS
N
IÑOS
T
RATADOS
EN
N
UESTRO
M
EDIO
CON
I
NFUSIÓN
S
UBCUTÁNEA
C
ONTINUA
DE
I
NSULINA
Figura 1: Indicaciones de ISCI.
Figura 2: Evolución de la HbA1c antes y durante ISCI.
PreISCI vs 1
año
PreISCI vs 2
años
PreISCI vs 3
años
p
0,947 (NS)
0,073 (NS)
0,737 (NS)
La dosis media de insulina diaria con múltiples dosis
de insulina fue de 0,89 ± 0,19 U/kg/día. Tras 1 año de
ISCI, los requerimientos diarios descendieron a 0,78 ±
0,17 U/kg/día. Al cabo de 2 años, fueron de 0,82 ±
0,19 U/kg/día. Finalmente, la dosis media en aquellos
pacientes que completaron 3 años de ISCI fue de 0,79
± 0,12 U/kg/día. Nuevamente, aunque se observan re-
querimientos menores de insulina en la terapia con ISCI
en comparación con el tratamiento con múltiples dosis
de insulina, la diferencia no es estadísticamente signifi-
cativa.
Figura 3: Evolución de la dosis diaria de insulina
antes y durante ISCI.
PreISCI vs 1
año
PreISCI vs 2
años
HbA1c preISCI
vs 3 años
p
0,067 (NS)
0,180 (NS)
0,052 (NS)
El índice de masa corporal tras iniciar tratamiento
con ISCI tampoco se modifica de forma estadística-
mente significativa en los pacientes de nuestra muestra
al cabo de 1, 2 y 3 años (figura 4).
Figura 4: Índice de masa corporal antes y durante
ISCI.
PreISCI vs 1
año
PreISCI vs 2
años
PreISCI vs 3
años
p
0,747 (NS)
0,499 (NS)
0,542 (NS)
El número de controles glucémicos capilares que
los pacientes se realizan al año de haber iniciado trata-
miento con bomba de insulina es significativamente su-
perior al realizado con la terapia previa de múltiples do-
sis (figura 5). No encontramos diferencias significativas
a los 2 y 3 años de tratamiento con ISCI.
Figura 5: Número de controles glucémicos capilares
antes y durante ISCI.
PreISCI vs 1
año
PreISCI vs 2
años
PreISCI vs 3
años
p
0,001
0,081 (NS)
0,097 (NS)
En todos los casos se mantuvo la terapia con ISCI
una vez instaurada con gran aceptación por parte del
paciente y sus cuidadores, exceptuando el caso de una
adolescente en la que, tras detectarse un trastorno de

20
S
OCIEDAD
DE
P
EDIATRÍA
DE
A
NDALUCÍA
O
CCIDENTAL
Y
E
XTREMADURA
Volumen XX Nº 2 Octubre 2013
la conducta alimentaria, se interrumpió el tratamiento
con bomba por indicación facultativa, regresándose a
la terapia con múltiples dosis de insulina.
Se registraron dos episodios de cetosis, sin acidosis,
secundarios a obstrucción en el equipo de infusión, no
resueltos en domicilio y en los que el paciente precisó
consultar en Urgencias. No se registraron episodios de
cetoacidosis. Durante el estudio, ninguno de los paci-
entes incluídos en la muestra analizada presentó una
hipoglucemia grave.
Discusión
El objetivo del tratamiento de la diabetes es conse-
guir y mantener un control glucémico lo más próximo
posible a la normalidad, sin incrementar el riesgo de hi-
poglucemia, para impedir o retrasar la aparición de las
complicaciones crónicas.
La terapia con ISCI ofrece en la práctica clínica ac-
tual la manera más fisiológica de aportar esta hormona.
Permite simular mejor el patrón normal de secreción
de insulina por la célula beta pancreática con la po-
sibilidad de administrar diferentes tipos de bolos para
cubrir las diversas ingestas o corregir hiperglucemias
ocasionales junto a la liberación continua de insulina
a lo largo de 24 horas (tasa basal) adaptándola a las
necesidades cambiantes del paciente.
El número de niños con DM1 tratados en las Uni-
dades de Diabetes de Cáceres y Badajoz en los últi-
mos 3 años ha sido 283. De estos, 44 han iniciado te-
rapia con bomba de insulina lo que supone un 15,5%
del total de niños con DM1 (el porcentaje real de pa-
cientes tratados con ISCI en nuestras unidades es de
hecho superior, pues pacientes que ya habían iniciado
tratamiento con ISCI antes de marzo de 2009 y aún en
seguimiento no han sido incluidos dentro del estudio).
Este porcentaje es muy superior a la media publicada
para nuestro país, situada en un 3-4% en 2011, y más
cercano al de los países de nuestro entorno social y
cultural
(9)
. Considerando la evidencia existente basada
en multitud de estudios, ensayos clínicos y meta-análi-
sis que avalan esta modalidad de terapia, continúa
siendo llamativa la infrautilización de la misma. Este
modesto uso de la ISCI en nuestro país podría atri-
buirse, al menos en parte, a un fenómeno de inercia
terapéutica
(11)
.
De acuerdo con el consenso internacional, todos los
pacientes pediátricos con DM1 son potenciales candi-
datos para la utilización de ISCI, sin limitación debido
a edad o momento evolutivo de la enfermedad, recay-
endo el inicio de la terapia en la decisión conjunta del
equipo diabetológico, el paciente y sus cuidadores. En
nuestro estudio, las hipoglucemias han constituido el
principal motivo para la indicación de ISCI seguida de la
inestabilidad glucémica. No obstante, debemos señalar
el hecho de que aunque ambos motivos constituyen,
en efecto, indicaciones reconocidas para iniciar ISCI, el
paciente y sus cuidadores han de ser apropiadamente
seleccionados y cumplir una serie de condiciones entre
las que se incluyen una alta motivación, expectativas
realistas, adecuado cumplimiento terapéutico, manejo
de la alimentación por raciones y determinación fre-
cuente de glucemia capilar. Asimismo, es fundamental
la disponibilidad de un equipo diabetológico con expe-
riencia en el tratamiento con ISCI
(13,14)
.
Son ya muchos los estudios que demuestran que
la utilización de ISCI en pacientes con DM1 se aso-
cia a un descenso en las cifras de HbA1c de 0,3-
0,6% cuando se compara con la administración de
MDI
(15,16,17,18,19)
. La magnitud de la reducción depende
de la cifra de partida de HbA1c, siendo los pacientes
con un valor previo más alto los que experimentan una
mayor disminución
(21)
. La mayoría de las publicaciones
sobre ISCI en la edad pediátrica son estudios no alea-
torizados que, como en nuestro trabajo, analizan di-
versas variables (HbA1c, IMC, frecuencia de hipogluce-
mias…) al pasar del tratamiento con MDI a ISCI
(21,22,23,24)
y muestran una reducción de la HbA1c alrededor del
0,6%. La principal limitación de estos estudios radica
en que el diseño retrospectivo y no randomizado im-
plica que los pacientes que inician ISCI habían dem-
ostrado previamente una motivación y cumplimiento
con MDI que previsiblemente mantendrían al pasar al
tratamiento con bomba. Las diferencias obtenidas en-
tre ISCI y MDI en diferentes estudios aleatorizados son
menos consistentes, si bien el número de pacientes en
muchos de estos estudios es pequeño y la duración
del estudio corta
(20,25,26,27)
. Un reciente estudio de ca-
sos-controles llevado a cabo en 345 pacientes durante
un tiempo medio de seguimiento de 3,5 años (±2,5
años), el de mayor tamaño muestral y duración hasta
la fecha, demuestra una reducción media de la HbA1c
de 0,6%. Esta diferencia en el grupo con ISCI se man-
tiene significativamente menor respecto al grupo con
MDI durante un tiempo de seguimiento de 7 años
(28)
.
En nuestro estudio, pese a la mejoría observada no
encontramos diferencias significativas en la HbA1c an-
tes y después inicio del tratamiento. Es interesante el
hecho de que la tendencia descendente que obser-
vamos en la cifra de HbA1c en nuestra muestra, que
inicialmente podría atribuirse a la reeducación diabe-
tológica, mayor motivación y seguimiento más es-
trecho, se mantiene también a los 2 y 3 años de segui-
miento. La HbA1c sí mejoró en el 60% de los paci-
entes en los que la principal indicación fue el mal con-
trol metabólico en términos de una elevada HbA1c.
Posiblemente, si la serie estudiada hubiera sido mayor
o el grupo más homogéneo en cuanto al motivo de
indicación podríamos haber encontrado la diferencia
publicada por otros autores (HbA1c 0,3-0,6% menor
en el grupo tratado con ISCI). Asimismo, la aceptable
HbA1c media de que partía nuestra serie también ten-
dería a minimizar esta diferencia pues, como ya hemos
señalado previamente, la mayor reducción en la HbA1c
al pasar a ISCI parece objetivarse en aquellos que

21
Volumen XX Nº 2 Octubre 2013
E
VALUACIÓN
DE
LOS
N
IÑOS
T
RATADOS
EN
N
UESTRO
M
EDIO
CON
I
NFUSIÓN
S
UBCUTÁNEA
C
ONTINUA
DE
I
NSULINA
parten de valores más altos. Por otro lado, considera-
mos insuficiente valorar el impacto de la ISCI sobre el
control glucémico tomando como única referencia la
HbA1c. En los últimos años, ha cobrado gran impor-
tancia el concepto de “memoria metabólica” y, aunque
aún en discusión, hay datos que relacionan la variabili-
dad glucémica con un incremento del riesgo de com-
plicaciones crónicas
(29)
. En este sentido, y teniendo en
cuenta que muchos de los pacientes que en nuestra
serie iniciaron ISCI presentaban una aceptable HbA1c
previa pero con gran fluctuación glucémica, creemos
importante el análisis de esta variable en futuros estu-
dios (por ejemplo, mediante empleo de monitorización
continua de glucosa).
En general, el tratamiento con ISCI implica una dis-
minución de la dosis de insulina diaria del paciente
(20,28,30)
. La tendencia observada en nuestro estudio
también sugiere menores requerimientos de insulina
con ISCI que con MDI. Este hallazgo parece relaciona-
rse con una mejor absorción de la hormona en la tera-
pia con ISCI debido a su administración fraccionada,
haciendo más previsible su efecto.
Aunque tras conocerse los resultados del DCCT,
surgió la preocupación sobre la posible ganancia pon-
deral con el tratamiento con ISCI, los estudios en po-
blación pediátrica no han corroborado dicho temor
(21,24,28)
. Tampoco en nuestro trabajo constatamos una
diferencia significativa en el IMC tras pasar del trata-
miento con MDI a ISCI. Si bien el tratamiento con ISCI
facilita la modificación del número de raciones en las
comidas (y, en consecuencia, proporciona una mayor
libertad para aumentar la ingesta), en la práctica tam-
bién reduce la necesidad de tentempiés al permitir una
adaptación más fisiológica en el aporte de insulina.
El aumento significativo en el número de glucemias
capilares diarias que observamos en nuestra serie du-
rante el primer año de tratamiento con ISCI parece
atribuible a la necesidad de un mayor autocontrol para
un mejor ajuste de tasas basales y una optimización
de la insulina prandial mediante el empleo de diferen-
tes tipos de bolos. Asimismo, la facilidad para adminis-
trar bolos correctores en caso de hiperglucemias oca-
sionales determinaría la necesidad de evaluar el efecto
de dichas correcciones mediante controles glucémi-
cos posteriores.
En la edad pediátrica, el impacto del tratamiento con
ISCI sobre las hipoglucemias es muy variable en los
diferentes estudios. Nuevamente, parecen observarse
mejores resultados en estudios no aleatorizados
(8,24,31)
,
con disminución del riesgo de hipoglucemia grave en
los pacientes tratados con ISCI. En cambio, los estu-
dios aleatorizados no muestran una diferencia significa-
tiva
(20,25,26,32,33,34)
. En nuestro estudio no nos propusimos
como objetivo la comparación del número de hipoglu-
cemias antes y después de iniciar tratamiento con ISCI
al considerar que carece de rigor metodológico con-
siderar únicamente las hipoglucemias anotadas en la
agenda o las halladas en las descargas del dispositivo.
Creemos que para realizar esta comparación es pre-
ciso un diseño más riguroso que incluyera la monitor-
ización continua de glucosa intersticial con objeto de
definir con mayor exactitud el tiempo de hipoglucemia.
En cualquier caso, ninguno de los pacientes de nues-
tra serie presentó una hipoglucemia grave durante el
tiempo de seguimiento tras inicio de ISCI.
En cuanto a los episodios de cetoacidosis, la aus-
encia de un depósito subcutáneo de insulina basal en
el tratamiento con ISCI incrementaría la susceptibili-
dad de cetosis primero, y cetoacidosis (CAD) posteri-
ormente, en caso de interrupción en el aporte contínuo
de insulina. Algunas revisiones (35,36) muestran estu-
dios con resultados discordantes y señala que, en caso
de aparecer, los episodios de CAD son más frecuentes
poco después de iniciar ISCI. Paradójicamente, tam-
bién describen un descenso del riesgo de CAD con
ISCI en pacientes con episodios previos recurrentes de
CAD, atribuible a la omisión previa de dosis con MDI y
al aporte continuo de insulina con la ISCI. En nuestro
estudio no se presentaron episodios de cetoacidosis
durante el seguimiento pero sí se registraron dos ca-
sos de cetosis (niveles de
?hidroxibutirato en sangre
? 0,5 mmol/L) secundaria a obstrucción del equipo de
infusión que el paciente y sus cuidadores no supieron
resolver, por lo que consultaron en Urgencias.
Las posibilidades que brinda la ISCI (adaptación a
las necesidades del paciente, administración de muy
bajas dosis de insulina, mejor cobertura de la ingesta
con diferentes tipos de bolos, disminución del número
de inyecciones diarias…) son percibidas por los niños,
cuidadores y familiares, y representan una mejoría en
su calidad de vida, siendo pocos los pacientes que
desean suspender este tipo de tratamiento una vez in-
staurado
(9)
. En nuestra serie, únicamente en una pa-
ciente se interrumpió el tratamiento con ISCI por indi-
cación del facultativo tras detectarse un trastorno de
la conducta alimentaria. Aunque nuestro estudio no ha
evaluado de una forma objetiva mediante el uso de
escalas el beneficio psicológico y el impacto sobre la
calidad de vida derivados de la ISCI, sí detectamos
en nuestra experiencia clínica, al igual que otros au-
tores
(26,30,37)
, la preferencia de pacientes y cuidadores
por esta forma de tratamiento y su deseo de continu-
arla. Se precisan estudios que evalúen estos aspectos
no sólo en pacientes que requieran terapia con ISCI
debido a las indicaciones mayoritariamente acepta-
das (mal control metabólico, inestabilidad glucémica,
fenómeno del alba…), sino también en aquellos con
un adecuado control previo. De este modo, y dejando
al margen el objetivo “glucocéntrico”, pacientes bien
controlados y que no reúnen ninguna de las indicacio-
nes consensuadas, podrían ser candidatos óptimos a
la ISCI tan sólo en aras de una mejoría en la calidad
de vida
(38,39)
.

22
S
OCIEDAD
DE
P
EDIATRÍA
DE
A
NDALUCÍA
O
CCIDENTAL
Y
E
XTREMADURA
Volumen XX Nº 2 Octubre 2013
En conclusión, el tratamiento con ISCI resulta en
nuestro estudio ser igual de efectivo que el tratamiento
con MDI en términos de HbA1c, demostrándose como
una alternativa adecuada, segura y bien aceptada en
pacientes previamente seleccionados. No obstante,
consideramos precisos nuevos estudios que evalúen
la efectividad de la ISCI mediante el análisis de otros
parámetros como varibalidad glucémica o calidad de
vida.
Los autores declaran que no existen conflictos de
intereses en relación con el contenido del presente
artículo.
Bibliografía
1. DCCT Research Group. The effect of intensive
diabetes treatment on the development and progres-
sion of long-term complications in insulin-dependent
diabetes mellitus. The Diabetes Control and Complica-
tions Trial. N Engl J Med. 1993;329:977-986.
2. DCCT Research Group. The effect of intensive
diabetes treatment on the development and progres-
sion of long-term complications in adolescents with
insulin-dependent diabetes mellitus: the Diabetes Con-
trol and Complications Trial. J Pediatr. 1994;125:177-
88.
3. Epidemiology of Diabetes Interventions and
Complications (EDIC). Design, implementation, and
preliminary results of a long-term follow-up of the Dia-
betes Control and Complications Trial cohort. Diabetes
Care. 1999; 22:99–111.
4. Battelino T. Risk and benefits of continous subcu-
taneous insulin infusion (CSII) treatment in school chil-
dren and adolescents. Pediatr Diabetes. 2006;7(Suppl.
4):20-24.
5. Pickup JC, Keen H, Parsons JA, Alberti KG. Con-
tinous subcutaneous insulin infusion. An approach to
achieving normoglycaemia. Br Med J. 1978;1.204-207.
6. Pickup JC, White MC, Keen H, Parsons JA,
Alberti KG. Long-term continous subcutaneous insulin
infusion in diabetic at home. Lancet. 1979;2:870-873.
7. Tamborlane WV, Sherwin RS, Genel , Felic P.
Reduction to normal of plasma glucose in juvenile dia-
betes by subcutaneous administration of insulin with a
portable infusion pump. N Engl J Med. 1979;300:573-
578.
8. Heidtmann B. insulinpumptherapie bei Kindern
und Jugendlichen. Therapieforum Diabetes. 2005;4:24-
27.
9. Hofer S, Meraner D, Koehle J. Insulin pump
treatment in children and adolescents with Type 1 dia-
betes. Minerva Pediatr 2012; Aug; 64(4):433-8
10. Renard E. Insulin pump use in Europe. Diabetes
Technol Ther. 2010; 12 (Suppl 1):29-32.
11. Conget I, Giménez M, Ampudia-Blasco FJ. Posi-
bles causas de la infrautilización de la infusión subcu-
tánea contínua de insulina en España. Av Diabetol.
2013;29(1):1-3.
12. Hernández M, Castellet J, Narvaiza J, Rincón J,
Ruiz I, Sánchez F, et al. Curvas y tablas de crecimiento.
Madrid: Garsi;1998.
13. Barrio R, García B, Gómez A, González I, Her-
moso F, Luzuriaga C, Oyarzabal M, Rica I, Rodríguez
M, Torres M. Documento de consenso sobre trata-
miento con infusión subcutánea continua de insulina
de la diabetes tipo 1 en la edad pediátrica. An Pediatr
(Barc). 2010;72(5): 352.e1-352.e4.
14. Phillip M, Battelino T, Rodriguez H, Danne T,
Kauffman F and Consensus Forum. Use of Insulin
Pump Therapy in the Pediatric Age-Group. Diabetes
Care 2007;30 (6): 1653-62.
15. Pickup JC, Sutton AJ. Severe hypoglycaemia
and glycaemic control in type 1 diabetes: meta-analysis
of multiple daily insulin injections compared with conti-
nous subcutaneous insulin infusion. Diabet Med. 2008;
25:765-74.
16. Pickup JC, Mattock M, Kerry S. Glycaemic con-
trol with continous subcutaneous insulin infusion com-
pared with intensive insulin injections in patients with
type 1 diabetes: meta-analysis of randomised contro-
lled trials. BMJ. 2002;234:705-11.
17. Weissberg-Benchell J, Antisdel-Lomaglio J, Ses-
hadri R. Insulin pump therapy: a meta-analysis. Dia-
betes Care. 2003; 26:1079-87.
18. Jeitler K, Horvath K, Berghold A. Continous sub-
cutaneous insulin infusion versus multiple daily insulin
injections in patients with diabetes mellitus: systematic
review and meta-analysis. Diabetología. 2008;51: 941-
51.
19. Pankowska E, Blaik M, Dziechaiarz P, Szypowska
A, Szajewka H. Continuos subcutaneous insulin infusion
vs multiple daily injections in children with type 1 dia-
betes: a systematic review and meta-analysis of rando-
mized control trials. Pedaitric diabetes 2009;10(1):52-8.
20. Wilson DM, Buckingham BA, Kunselman EL,
Sullivan MM, Paguntalan HU, Gitelman SE. A two-
center randomized controlled feasibility trial os insulin-
pump therapy in young children with diabetes. Diabetes
Care. 2005;28:15-9.
21. Ahern JA, Boland EA, Doane R, Ahern JJ, Rose
P, Vincent M, Tamborlane WV. Insulin pump therapy
in pediatrics: a therapeutic alternative to safely lower
HbA1c levels across all age groups. Pediatr Diabetes.
2002;3:10-5.
22. Maniatis AK, Klingensmith GJ, Sloveer RH,
Mowry CJ, Chase HP. Continous subcutaneous insulin
infusion therapy for children and adolescents. An option
for routine diabetes care. Pediatrics. 2001;74:217-21.
23. Plotnick LP, ClarK LM, Brancati FL, Erlinger T.
Safety and effectiveness of insulin pump therapy in chil-

23
Volumen XX Nº 2 Octubre 2013
E
VALUACIÓN
DE
LOS
N
IÑOS
T
RATADOS
EN
N
UESTRO
M
EDIO
CON
I
NFUSIÓN
S
UBCUTÁNEA
C
ONTINUA
DE
I
NSULINA
dren and adolescents with type 1 diabetes. Diabetes
Care. 2003;26:1142-6.
24. Weinzimer S, Swan K, Sikes K, Ahern JA. Emer-
ging evidence for the use of insulin pump therapy in
infants, toddlers, and preschool-aged children with
type 1 diabetes. Pediatric Diabetes. 2006; 7(Suppl
4):15-19.
25. DiMeglio LA, Pottorff TM, Boyd SR, France L,
Fineberg N, Eugster EA. A randomized controlled study
of insulin pump therapy in diabetic preschoolers. J
Pediatr. 2004; 145280-84.
26. Fox LA, Buckloh LM, Smith SD, Wysocki T,
Mauras N. A randomized controlled trial of insulin the-
rapy in young children with type 1 diabetes mellitus.
Diabetes care. 2005;28:1277-81.
27. Batajoo RJ, Messina CR, Wilson TA. Long-term
efficacy of insulin pump therapy in children with type
1 diabetes mellitus. J Clin Res Pediatr Endocrinol
2012;Sep;4(3):127-31.
28. Johnson SR, Cooper MN, Jones TW, Davis EA.
Long-term outcome of insulin pump therapy in children
with type 1 diabetes assessed in a large population-
based case-control study. Diabetología. 2013;56.
29. Ceriello A, Ihnat MA. Glycaemic Variability: a new
therapeutic challenge in diabetes and the critical care
setting. Diabetes Med. 2010;27:862-67.
30. Nicoljsen T, Samuelsson A, Hanas r. Insulin doses
before and one year after pump star: Children have a
reserved dawn phenomenon. J Diabetes Sci Techno-
logy 2012; May1; 6(3):589-94.
31. Hannaire-Broutin H, Melki V, Bessieres-Lacombe
S, Tauber JP. Comparison of subcutaneous insulin
infusion and multiple dail injection regimens using
insulin lispro in type 1 diabetic patients on intensified
treatment: a randomized study. The Study Group for
the Development of Pump Therapy in Diabetes. Dia-
betes Care- 2000;23:1232-5.
32. Weintrob N, Schechter A, Benzaquen H, Shalitin
S, Lilos A, Galatzer A, et al. Glycemic patterns detected
by continous subcutaneous glucose sensing in chil-
dren and adolescents with type 1 diabetes mellitus
treated by multiple daily injections vs continous sub-
cutaneous insulin infusion. Arch Pediatr Adolesc Med.
2004;158:677-84.
33. Cohen D, Weintrob N, Benzaquen H, Galatzer A,
Fayman G, Phillip M. Continous subcutaneous insulin
infusion versus multiple daily injections in adolescents
with type 1 diabetes mellitus: a randomized open cros-
sover trial. J Pediatr Endocrinol Metab. 2003;16:1047-
50.
34. Doyle EA, Weinzeimer SA, Steffen AT, Ahern JA,
Vincent M, tamborlane WV. A randomized prospective
trial comparing the efficacy of continous subcutaneous
insulin infusion with multiple daily injections using insulin
glargine. Diabetes Care;7 (Suppl. 4):11-4.
35. Hanas R, Ludvigsson J. Hypoglycemia and
ketoacidosis with insulin pump therapy in children and
adolescents. Pediatric Diabetes. 2006;7(Suppl. 4):32-
38.
36. Cope JU, Samuels-Reid JH, Morrison AE.
Pediatric use of insulin pump technology: a retros-
pective study of adverse events in children ages 1-12
years. J Diabetes Science Technology. 2012; Sep 1;
6(5):1053-9.
37. Word JR, Moreland EC, Volkening LK, Sobren
BM, Butler DA, Laffel LMB. Durability of insulin pump
use in pediatric patients with type 1 diabetes. Diabetes
Care. 2006;29:2355-60.
38. Hirose M, Bewerly EA, Weigner K. Quality of life
and technology: impact on children and families with
diabetes. Curr Diab Rep 2012; Dec;12(6):711-20.
39. Pickup JC. Insulin-pump therapy for type 1
diabetes mellitus. New England Journal of Medicine.
2012;366:1616-24.
| Adjunto | Tamaño |
|---|---|
| voxpaed2.2pags16-23.pdf | 226.96 KB |



